Укротители макрофагов.
Как работает Лаборатория трансляционной клеточной и молекулярной биомедицины?
Можно ли перепрограммировать иммунную систему и как это поможет победить рак и инфаркт миокарда? Как добиться того, чтобы имплантаты не вызывали отторжения в организме? Почему большие проекты можно осуществлять только в кооперации?
Сегодня рассказываем об еще одной лаборатории, которая вошла в состав томского Центра биомедицины и биотехнологий. Здесь биологи и химики ТГУ, врачи и ученые СибГМУ, специалисты из Томского НИМЦ — НИИ онкологии, НИИ кардиологии и других научных учреждений Томска под научным руководством д.б.н., профессора Юлии Кжышковской учатся «укрощать» главные клетки иммунной системы — макрофаги.
Центр биомедицины и биотехнологий, создаваемый в Томске, объединит ресурсы томских университетов — ТГУ, ТПУ, ТУСУР, а также НИМЦ и нескольких НИИ. Внутри него запустят Центр коллективного пользования, лаборатории и образовательное пространство.
Такой проект — очередной шаг на пути трансформации традиционных структур, когда на волне технологических инноваций формируется «гринфилд», «зеленое поле», существующее параллельно привычным институтам. Этот термин определяет освоение нового пространства, где создается новая инфраструктура и возможность для реализации проектов «с нуля». Создаваемые на нем образовательные стартапы получили название «EdTech»-проекты.
Клетка меняет профессию

Когда макрофаги-пожиратели, авангард нашей иммунной системы, начинают неадекватно реагировать на угрозы — не обращать внимания на опасных интервентов или поддерживать внутренних врагов — это становится причиной опасных болезней, вплоть до онкологии и инфаркта миокарда.
Отторжение имплантатов тоже происходит из-за агрессивного поведения макрофагов. Научившись перепрограммировать эти клетки, а также создавать материалы, неуязвимые для их «зубов», можно победить многие ныне смертельные заболевания. Вот основная научная идея, на которой строится работа лаборатории трансляционной клеточной и молекулярной биомедицины.
Работая с клетками врожденного иммунитета, наша научная группа из НИИ онкологии изучает механизмы развития и устойчивости к терапии рака молочной железы, гортани и желудка. Кардиологи работают с клетками и тканями сердечной мышцы, а химики и материаловеды разрабатывают имплантаты, которые идеально подходили бы для организма каждого конкретного пациента. Но научная гипотеза, которая лежит в основе одна.
Макрофаги присутствуют в нашем организме с рождения, и при необходимости образуются (дифференцируются) в течение всей жизни из особых клеток крови — моноцитов. Они находятся во всех тканях нашего организма и заботятся об их ежедневной нормальной жизни.
При возникновении опасной ситуации, макрофаги могут пойти по двум разным путям развития — это называется дифференцировкой и активацией. Один путь вызывает острый иммунный ответ, который позволяет быстро справиться с бактериальной атакой и заживить рану, но при этом может вызвать отторжение имплантата. Второй путь, наоборот, сдерживает иммунную систему, снижает интенсивность воспалительного процесса, но это тоже не всегда хорошо: макрофаги могут вовремя не отреагировать, например, на трансформацию нормальной клетки в опухолевую, которая должна быть уничтожена, и «пропустить» ее.
— Идеальный результат, к которому мы стремимся в перспективе — перепрограммировать макрофаги, задавать им пути дифференцировки и активации, — поясняет Елена Чурина, доктор мед. наук, профессор ТГУ и СибГМУ, врач иммунолог-аллерголог, которая также работает над проектом лаборатории. — Используя препараты рекомбинантных цитокинов (белков, которые регулируют дифференцировку макрофагов), мы сможем достигать нужного эффекта. В идеале мы можем ввести этот белок непосредственно в клеточное микроокружение или в клетку в структуре опухолевой ткани, либо очага воспаления, и задать макрофагам то направление дифференцировки, которое нам нужно. Но необходимо разработать систему адресной доставки препарата. Это тоже актуальная проблема, здесь нужны биодеградируемые полимерные материалы (микрокапсулы), остатки которых должны быть удалены из организма теми же макрофагами, после осуществления доставки.
От инфаркта и от рака
Направленная дифференцировка макрофагов может помочь при многих заболеваниях. Например, процесс восстановления после инфаркта миокарда также зависит от особенностей иммунной системы. Макрофаги начинают действовать, когда поврежденные клетки сердечной мышцы становятся чужеродными для организма. Формируется воспалительный ответ, вызывающий рубцовые изменения с развитием сердечной недостаточности в дальнейшем.
Ученые из томского НИИ кардиологии установили, что степень воспаления и рубцовых изменений не всегда находятся в прямой зависимости от площади поражения миокарда.
— Уникальность наших совместных с коллегами из кардиоцентра исследований в том, что они проводятся на аутопсийном материале: сердцах людей, умерших от инфаркта миокарда разной степени тяжести», — объясняет Елена Чурина. — Наши сотрудники и магистранты изучают клеточный состав срезов сердечной мышцы, и это позволяет сделать вывод, какие клетки пришли туда в момент развития иммунного ответа и воспалительного процесса.
Выяснилось, что иногда при большой площади первоначального повреждения рубцовые изменения минимальные, а бывает наоборот: инфаркт не крупноочаговый, но затем происходит активное деление клеток соединительной ткани, образующей рубец. Сердце уже не может эффективно выполнять свою насосную функцию, прогрессирует сердечная недостаточность и человек умирает. Хорошая новость в том, что эти процессы можно регулировать, уменьшая интенсивность иммунного ответа.
В случае с онкологическими заболеваниями история другая. Раковые клетки умеют «обманывать» макрофаги, и они, вместо того, чтобы убивать агрессивные опухолевые клетки (то есть формировать иммунный ответ по защитному типу) начинают помогать им. В этом случае требуется перепрограммировать макрофаги таким образом, чтобы вызвать максимальную активацию иммунного ответа, помогающую лечению. Иммунотерапия онкологических заболеваний — единственная надежда на успех в борьбе против опухолевых клеток.
Имплантаты с индивидуальностью

Еще одна проблема современного мира — приживаемость имплантатов. Люди научились заменять в организме многое — от зубов до сердечных клапанов — но часто организм воспринимает имплантаты как чужеродный элемент и попросту отторгает. В этом тоже принимают участие макрофаги.
— Может быть, вы обращали внимание, что если не вытаскивать занозу, то начнется воспалительный процесс, и в конечном счете она просто растворится. Ее «съедят» макрофаги, — говорит заместитель заведующей лабораторией Ирина Курзина. — Точно так же макрофаги пытаются поглотить и имплантаты. Есть томографические исследования, на которых буквально видны макрофаги с молекулами гидроксиапатита внутри, материала, из которого изготавливают имплантаты. Причем, иммунная система каждого человека реагирует индивидуально. У одного имплантаты приживаются, у других вызывают острую воспалительную реакцию. Все происходит на клеточном уровне, эти механизмы нуждаются в дальнейших исследованиях.
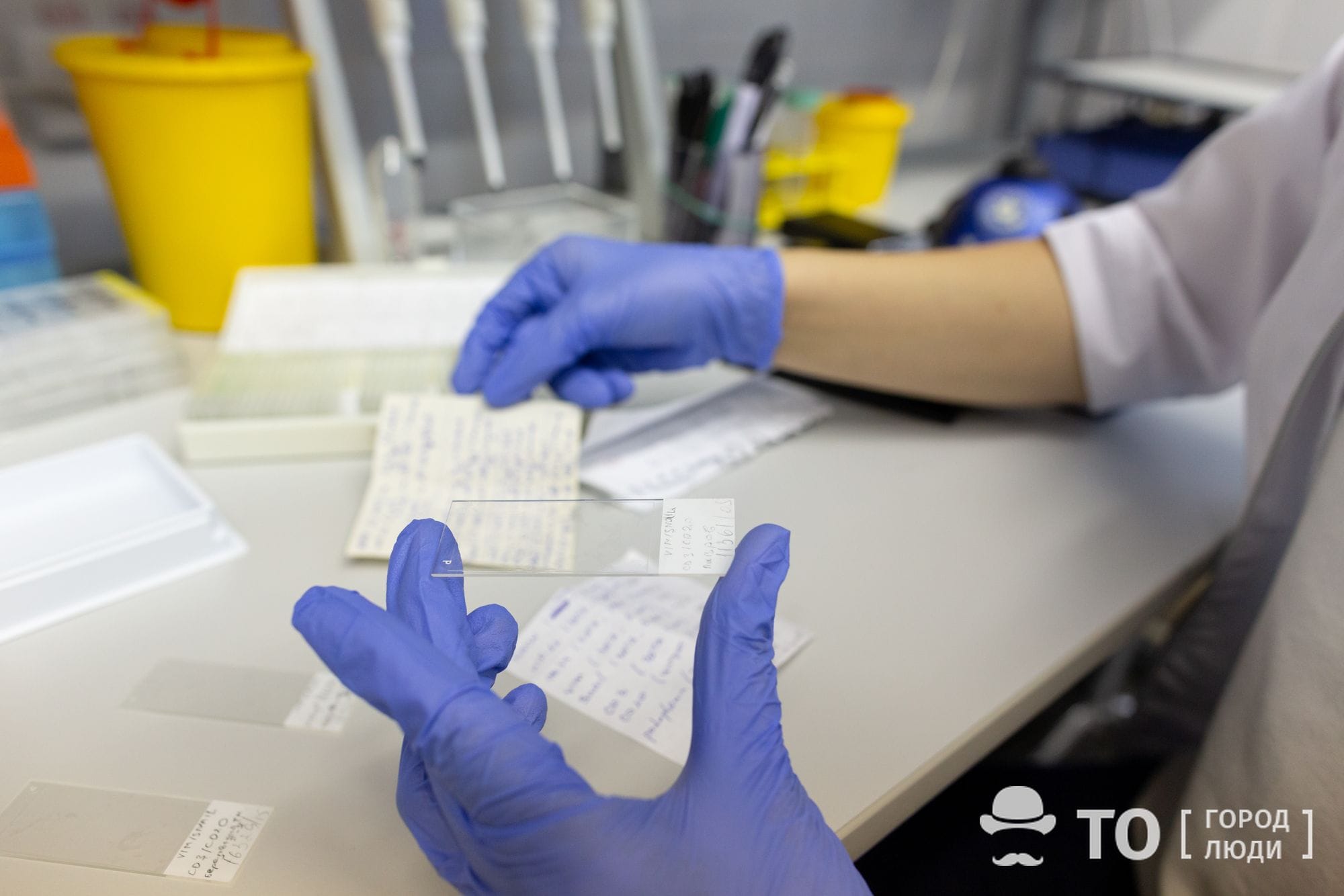
Как показывают научные исследования и клинический опыт, имплантаты из одного и того же материала у разных пациентов вызывают абсолютно разный иммунный ответ. Не существует такого материала, который подходил бы всем универсально. Казалось бы, химический состав имплантата одинаковый, но реакция иммунной системы на него непредсказуема — она совершенно разная.
— Когда некоторые физики и химики обещают разработать абсолютно толерогенный материал, то есть такой, который вообще не вызовет реакции иммунной системы, к сожалению, они лукавят, этого никогда не произойдет, — уверена иммунолог Елена Чурина. — Наша иммунная система эволюционно сформировалась таким образом, что распознает любой антиген и реализует на него свой ответ в любом случае. Наша задача — модифицировать поверхность материала, либо придать ей дополнительные свойства, чтобы свести патологические эффекты иммунного ответа к минимуму. Вот это и будут толерогенные материалы, которые ограничивают возникновение острого воспаления и отторжения имплантата.
То есть, прежде чем внедрять имплантат в организм, нужно протестировать материал с помощью макрофагальной тест-системы из собственных макрофагов пациента и подобрать такой вариант, который подходит именно для него. И это тот самый подход к лечению, который называется персонализированной медициной.
Трансдисциплинарность в тренде

Как подразделение университета, лаборатория занимается обучением студентов. Впрочем, этим она будет заниматься и в составе нового Центра биомедицины и биотехнологий, где будет создана Школа инженерной биологии.
При лаборатории и САЕ «Умные материалы и технологии» разработана и реализована уникальная междисциплинарная магистерская программа, «Трансляционные химические и биомедицинские технологии». Кроме глубоких знаний в различных областях химии, магистранты осваивают основы клеточной биологии, общей иммунологии, биохимии и других биомедицинских дисциплин.
— Сейчас в тренде трансдисциплинарные исследования», — говорит одна из разработчиц магистерской программы и ее преподаватель Елена Чурина. — Специалисты, которые работают на стыке наук уже сейчас высоко востребованы на рынке труда, и вообще, я считаю, что за ними будущее. Мы вполне довольны тем, как реализуется магистерская программа. В прошлом году было набрано 10 человек, в этом году — 11, и это достаточно высокий показатель, так как часто на автономных магистерских программах и по 2 — 3 человека учится. А в перспективе хотелось бы, конечно, еще и деньги зарабатывать на этом, принимать платных студентов.
 Практику магистранты проходят, в основном, на базе организаций-партнеров лаборатории, в ключевых институтах Томского НИМЦ, прежде всего, в НИИ онкологии и НИИ кардиологии. Там у студентов есть возможность поработать на уникальном современном оборудовании, клиническом и секционном материале, непосредственно взаимодействовать с врачами и высококвалифицированными научными сотрудниками.
Практику магистранты проходят, в основном, на базе организаций-партнеров лаборатории, в ключевых институтах Томского НИМЦ, прежде всего, в НИИ онкологии и НИИ кардиологии. Там у студентов есть возможность поработать на уникальном современном оборудовании, клиническом и секционном материале, непосредственно взаимодействовать с врачами и высококвалифицированными научными сотрудниками.
Магистранты двух предыдущих выпусков находят себя в науке. Кто-то остается работать в лаборатории и поступает в аспирантуру, кто-то идет в научно-исследовательские институты, кто-то уезжает в другие регионы и страны.
Плюсы кооперации

Тема, которой занимаются ученые лаборатории трансляционной клеточной и молекулярной биомедицины, настолько масштабна и сложна, что одному научному коллективу ее не осилить. Получить заметные научные результаты можно только в коллаборации с учеными разных специальностей и при объединении приборной базы научных организаций.
Лаборатория изначально, в 2014 году, создавалась как своего рода консорциум: в ней работают не только сотрудники классического и медицинского университетов, но и ученые из Томского НИМЦ. Также в этих организациях есть площади, закрепленные за лабораторией; такая структура в западной традиции называется «зеркальной». Но в своем стремлении к кооперации лаборатория идет дальше. С этого года она также стала одной из ключевых лабораторий Центра биомедицины и биотехнологий, созданного в городе Томске.
— Сейчас мир строится таким образом, что каждый сохраняет свою самостоятельность, но входит в какие-то альянсы, — поясняет Ирина Курзина. — Раньше структура университета была феодальной: факультет, в его составе кафедры, затем лаборатории, и все подчиняются идеологии деканата и ученого совета. Это уже не работает, сейчас более открытые организации и платформенные структуры.
Как и коллеги из лаборатории нейробиологии ТГУ ученые будут заниматься подготовкой студентов и научной работой, и, соответственно, пользоваться ресурсами Центра коллективного пользования и других научных организаций, входящих в консорциум.
Из необходимого для работы лаборатории оборудования, которое уже имеется в центре коллективного пользования или планируется к приобретению — более широкая линейка секвенаторов ДНК. Но главное — там будут чистые зоны, где исключено присутствие загрязняющих частиц и микроорганизмов, потому что сейчас площади лаборатории не позволяют оборудовать такое помещение. Исследования, для которых необходимы стерильные условия, сегодня реализуются на площадях НИИ онкологии.
— Это даст нам возможность участвовать в больших и серьезных научных проектах, — отвечают на вопрос о преимуществах вхождения в Центр биомедицины Юлия Кжышковска и Ирина Курзина. — Мы как лаборатория можем работать над отдельными вопросами, но не можем решать широкие совокупности задач, потому что у нас для этого может быть недостаточно компетенций или приборной базы. А когда кооперируется несколько лабораторий, в этом альянсе можно получить доступ к серьезному проекту, финансированию, к приборной базе. Объединившись, мы получаем больше, чем по отдельности.
Текст: Катерина Кайгородова

